Por meses e meses, o que mais tínhamos em nossas mentes quando o assunto Pandemia vinha à tona eram perguntas e mais perguntas. Por exemplo, o vírus é mortal? Como sei que estou infectado? Há uma cura? Quanto tempo será de lockdown? Preciso usar máscara e álcool em gel? Quando vai haver uma vacina? Tem algum remédio? Como as vacinas funcionam? Quanto tempo dura a proteção gerada por elas? E as variantes? Posso me infectar e transmitir mesmo vacinado? Como acontece a transmissão?
Mês a mês, pesquisa após pesquisa, fomos aprendendo e descobrindo um pouco mais sobre o SARS-CoV-2, a COVID-19, as variantes e as vacinas.
Mas ainda assim, duas perguntas ressoavam no fundo de nossas mentes, nos fazendo repeti-las a cada nova descoberta: por quanto tempo a imunidade das vacinas dura e, mesmo vacinado, ainda posso infectar novas pessoas?
Bem, logo de cara posso lhes dizer que ainda não temos certeza de quanto tempo a imunidade total das vacinas dura em nosso corpo. Temos algumas noções, vários estudos avaliando o número de anticorpos, com muitas pesquisas mostrando a redução dos anticorpos após vários meses (o que é algo totalmente normal olhando do ponto de vista imunológico), mas ainda um baixo número de artigos avaliando a resposta imune celular, isso é, a porção do nosso sistema imune que nos defende utilizando células.
Entretanto, quanto ao impacto das vacinas na transmissão, temos cada vez mais informações que nos auxiliam em montar um panorama geral sobre esse assunto. E é sobre isso que vamos falar aqui hoje.
O que se sabe até o momento sobre a influência das vacinas na transmissão da COVID-19?
Pouco tempo após as primeiras campanhas de vacinação ao redor do mundo terem começado, os primeiros estudos avaliando sua capacidade de reduzir os sintomas da COVID-19, hospitalizações e mortes eram publicados. Nessa época, muitos desses estudos chegavam a comentar sobre a possibilidade das vacinas estarem reduzindo a transmissão do SARS-CoV-2 entre as pessoas. Contudo, esses primeiros estudos não focaram em avaliar exatamente a transmissão entre as pessoas. Por causa disso, muitas dessas suposições sobre o impacto na transmissão ficavam no campo das ideias.
Entretanto, já passou um ano de vacinação mundo afora. Assim, vários estudos foram feitos focando especificamente no impacto da vacinação na transmissão, avaliando e mostrando efeitos bem positivos. Tudo isso reafirma a necessidade do uso de vacinas (mas não exclusivamente o uso delas) para se chegar ao fim da pandemia.
Entre muitas coisas, esses são os principais pontos que sabemos no momento:
- As vacinas reduzem a infecção inicial causada pelo SARS-CoV-2. Isto é, os sintomas sentidos por uma pessoa totalmente vacinada infectada tendem a ser mais leves, do que em uma pessoa não vacinada infectada;
- O tempo levado pelo vírus para gerar uma cópia de si mesmo dentro das nossas células (chamado de tempo de replicação) é menor em pessoas totalmente vacinadas que se infectaram. Isto quando comparado com pessoas não vacinadas infectadas. Consequentemente, a quantidade de vírus no organismo (a carga viral) de uma pessoa totalmente vacinada infectada é menor;
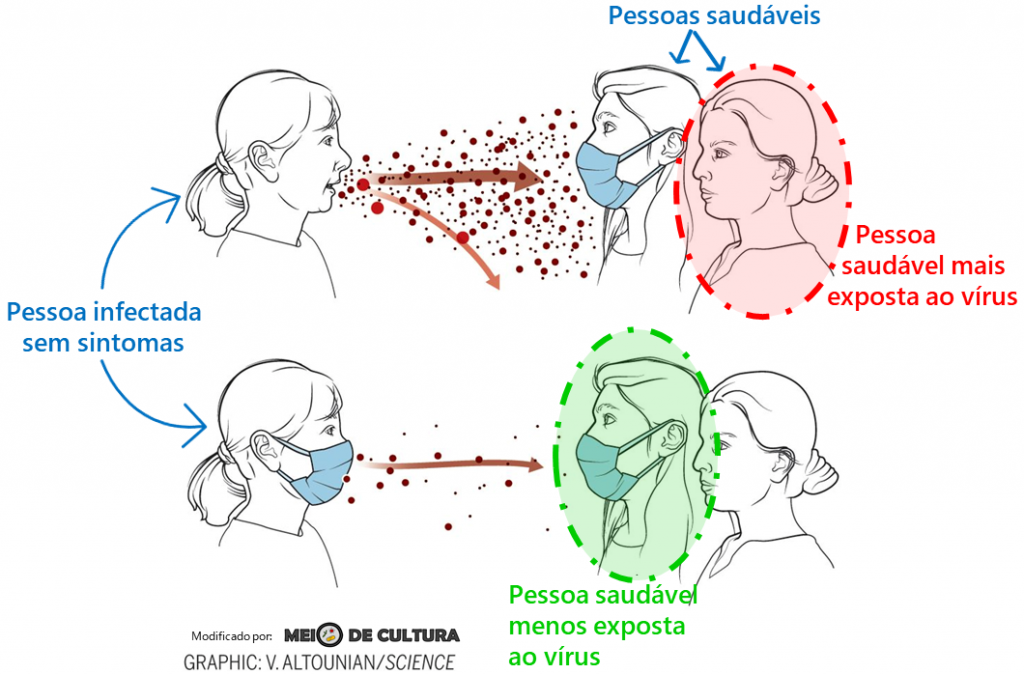
- Pessoas totalmente vacinadas infectadas emitem uma quantidade menor de partículas virais através de tosse, espirro ou mesmo a fala. Além disso, as partículas virais emitidas por essas pessoas têm uma infecciosidade menor.
- Em outras palavras, uma pessoa totalmente vacinada e que foi infectada joga para fora do seu corpo uma quantidade menor de vírus, e esses vírus têm também uma menor capacidade de infectar outra pessoa;
- Pessoas totalmente vacinadas que foram infectadas pelo SARS-CoV-2 conseguem limpar o vírus do seu corpo mais rapidamente. Isto é, o sistema imune desses indivíduos é mais eficiente em matar os vírus e as células infectadas por ele, em um intervalo de tempo menor.
Ok, em um grande resumo, o que isso quer dizer?
Todos esses dados nos mostram que vacinas foram e são capazes de reduzir o tempo que o vírus fica dentro de nosso corpo, a partir de várias formas que é REDUZINDO:
- a multiplicação do vírus;
- a sua emissão;
- o tempo que o vírus fica dentro do corpo;
Assim sendo, de forma indireta, é possível dizer que as vacinas impactam e reduzem sim a transmissão do SARS-CoV-2 em pessoas totalmente vacinadas.
E se você chegou aqui e ainda tem dúvidas sobre isso, vamos pensar o seguinte:
“Se uma pessoa com COVID-19 têm menos vírus dentro do corpo (por esse não estar conseguindo se multiplicar rapidamente), tal pessoa emite menos vírus para o ambiente ao seu redor (por tossir e espirrar menos, por exemplo) e fica menos tempo com o vírus dentro do corpo (por seu sistema imune estar matando o vírus e as células infectadas mais rápido). Assim, essa pessoa tem uma chance menor de transmitir o vírus para outros indivíduos, quando comparada com um indivíduo que se infectou sem estar vacinado.”
Aqui é o momento em que faço algumas ressalvas. Note bem a palavra que foi usada anteriormente: indivíduos vacinados têm uma chance MENOR de transmitir para outras pessoas. Isso não quer dizer que, se você foi vacinado com duas ou três doses, você não terá chance alguma de pegar e transmitir o SARS-CoV-2.
Além disso, uma segunda ressalva que devo fazer aqui é sobre esses mesmos estudos que citei: as pesquisas mais completas avaliaram a transmissão de pessoa para pessoa em contatos domiciliares, e não em grandes ambientes abertos ou com grandes aglomerações. Para essas situações, novamente, ainda é estritamente necessário que nós continuemos a utilizar medidas não farmacológicas, como o uso de máscaras e de distanciamento social, em ambientes fechados ou com grandes quantidade de pessoas.
O grande ponto da discussão aqui é: uma pessoa com o esquema vacinal completo tem uma menor PROBABILIDADE de conseguir transmitir o vírus para outra pessoa. As vacinas não param a transmissão, mas sim reduzem esta.
Além disso, como tem se falado muito, as vacinas também garantem outras vantagens como:
- A redução da chance de desenvolver doença grave, hospitalização e morte por COVID-19;
- A intensidade dos sintomas sentidos após o fim da COVID-19 de longa duração (que também têm sido chamadas de Sequelas Pós-COVID)
- E também mas não menos importante, a frequência que variantes de preocupação surgem;
Ué, mas ouvi dizer que as vacinas ajudam no surgimento de novas variantes
Pois bem, já vou dar a resposta mais simples, curta e direta para esse tipo de boato que foi veiculado recentemente: Não. Vacinas não ajudam no surgimento de novas variantes. Ponto.
Agora que já deixamos isso certo, vem entender melhor comigo o motivo.
Durante uma infecção, seja por um vírus, bactéria, fungo, ou qualquer outro parasita, nosso corpo trava um cabo de guerra: nosso sistema imune contra o parasita em questão (no caso, o SARS-CoV-2). Para fugir das diversas defesas que o sistema imune possui, os vírus possuem utilizam de sua maior arma: sua alta capacidade de mutação.
A mutação é nada menos que uma troca em alguma das bases nitrogenadas (as famosas “letrinhas”) no material genético, durante o processo de replicação. Entretanto, esse processo é caro, pois somente poucas mutações serão benéficas, enquanto que a grande maioria das mutações que surgirem irão ser, de alguma forma, ruins para o organismo em questão (no caso, o vírus).
O modo de se contornar esse problema é relativamente simples: infectando mais pessoas, ou, em outras palavras, se transmitindo mais. Quanto mais pessoas são infectadas (alta transmissibilidade), mais vírus são mutados, e maior é a chance de aparecer uma mutação que seja boa para ele (e, consequentemente, ruim para nós). Quando uma mutação boa aparece, esse vírus consegue se transmitir mais fácil, infectar mais pessoas, ganhar mais mutações, e isso acaba se tornando um ciclo eterno.
Dessa forma, surge a pergunta: como reduzir o número de mutações?
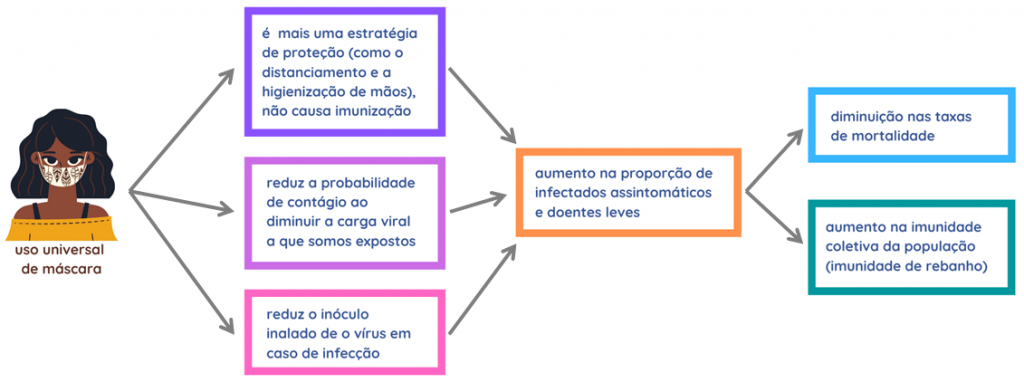
E a resposta mais simples (que, a propósito, já temos falado há bastante tempo) é: reduzindo a transmissão do vírus entre as pessoas. Para isso, precisamos utilizar tanto medidas farmacológicas quanto não farmacológicas. Por isso a importância do uso combinado de máscaras, álcool em gel, distanciamento social E vacinas. As três primeiras medidas vão atuar logo no começo de uma cascata de eventos (citada logo mais), enquanto a vacina atua a partir do meio dela. A seguir exemplificamos como todas essas medidas auxiliam na redução da transmissão e, consequentemente, reduzem o surgimento de novas variantes.
Vacinação em massa e uso de medidas não farmacológicas → Menos pessoas se infectando → pessoas que foram infectadas tendo um tempo de infecção menor → Com o tempo de infecção menor, o vírus fica menos tempo no corpo do indivíduo → Quanto menor o tempo que o vírus fica no corpo do indivíduo, menor a quantidade de vírus se multiplicando ali → Quanto menor a quantidade de vírus se multiplicando, menor a quantidade de mutações aparecendo → Quanto menor a quantidade de mutações aparecendo, menor a chance de surgir uma variante mais transmissível.
Finalizando
O ponto central aqui é mostrar que somente uma medida (como a vacinação de parte da população), não será o suficiente para acabarmos com a pandemia. Se quisermos que ela realmente chegue ao fim, precisamos todos fazer um esforço em conjunto para reduzir a transmissão do vírus, com a vacinação de TODA a população global, aliado ao uso de máscara, distanciamento social e – quando necessário – quarentena. Somente assim seremos capazes de diminuir o surgimento de novas variantes e superar a pandemia de uma vez por todas.
Para saber mais:
- Kissler, SM, Fauver, JR, Mack, C, Tai, CG, Breban, MI, Watkins, AE, … & Grad, YH (2021) Viral dynamics of SARS-CoV-2 variants in vaccinated and unvaccinated persons, New England Journal of Medicine, 385(26), 2489-2491.
- Heitmann, JS, Bilich, T, Tandler, C, Nelde, A, Maringer, Y, Marconato, M, … & Walz, JS (2021) A COVID-19 peptide vaccine for the induction of SARS-CoV-2 T cell immunity, Nature, 1-9.
- Lowe, D (2021) Vaccines Will Not Produce Worse Variants Science.
- Mostaghimi, D, Valdez, CN, Larson, HT, Kalinich, CC, & Iwasaki, A (2021) Prevention of host-to-host transmission by SARS-CoV-2 vaccines, The Lancet Infectious Diseases.
- Mlcochova, P, Kemp, SA, Dhar, MS, Papa, G, Meng, B, Ferreira, IA, … & Gupta, R. K (2021) SARS-CoV-2 B.1.617.2 Delta variant replication and immune evasion, Nature, 599(7883), 114-119.
- Kupferschmidt, K (2021) Evolving threat, Science.
- Roberts, M (2021) Covid: Double vaccinated can still spread virus at home, BBC.
- O’Hare, R (2021) COVID vaccines effective but household transmission of delta a risk for 1 in 4, Imperial College London.
- Singanayagam, A, Hakki, S, Dunning, J, Madon, KJ, Crone, MA, Koycheva, A, … & Lackenby, A (2021) Community transmission and viral load kinetics of the SARS-CoV-2 delta (B.1.617.2) variant in vaccinated and unvaccinated individuals in the UK: a prospective, longitudinal, cohort study, The Lancet Infectious Diseases.
- Alford, J (2021) Coronavirus infections three times lower in double vaccinated people – REACT, Imperial College London.
Outros Materiais:
- Mellanie Fontes-Dutra
Vacinas impactam na transmissão;
Vacinas podem produzir variantes mais resistentes? Não!;
Vacinação reduz transmissão de delta e individuos vacinados transmitem menos;
Este texto foi escrito originalmente para o Especial COVID-19.

Os argumentos expressos nos posts deste especial são dos pesquisadores. Dessa forma, produziu-se textos produzidos a partir de campos de pesquisa científica e atuação profissional dos pesquisadores. Além disso, a revisão por pares aconteceu por pesquisadores da mesma área técnica-científica da Unicamp. Assim, não, necessariamente, representam a visão da Unicamp e essas opiniões não substituem conselhos médicos.